CD163-პოზიტიური მაკროფაგების ექსპრესიის თავისებურებები საკვერცხის სეროზული სიმსივნეების პერიტონეუმის იმპლანტებში: ციფრული პათოლოგიის რაოდენობრივი კვლევა
ჩამოტვირთვები
სიმსივნის პერიტონური დისემინაცია საკვერცხის ეპითელური სიმსივნეების კრიტიკულად მნიშვნელოვანი მახასიათებელია და განსაზღვრულ როლს ასრულებს დაავადების პროგრესირებასა და არახელსაყრელ კლინიკურ გამოსავალში. სულ უფრო მეტი მტკიცებულება მიუთითებს, რომ სიმსივნის მიკროგარემო, განსაკუთრებით სიმსივნესთან ასოცირებული მაკროფაგები, მნიშვნელოვნად უწყობს ხელს მეტასტაზურ ქცევას. CD163 არის M2-პოლარიზებული მაკროფაგების კარგად დამკვიდრებული მარკერი, რომელიც დაკავშირებულია იმუნოსუპრესიასთან და სიმსივნის ხელშეწყობასთან. თუმცა, CD163-დადებითი მაკროფაგების სივრცითი განაწილება და რაოდენობრივი მახასიათებლები საკვერცხის სეროზული სიმსივნეების პერიტონურ იმპლანტებში ჯერ კიდევ არასაკმარისად არის შესწავლილი.
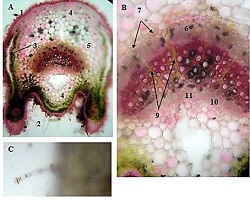
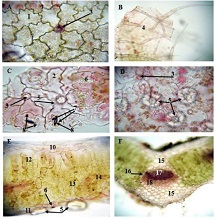
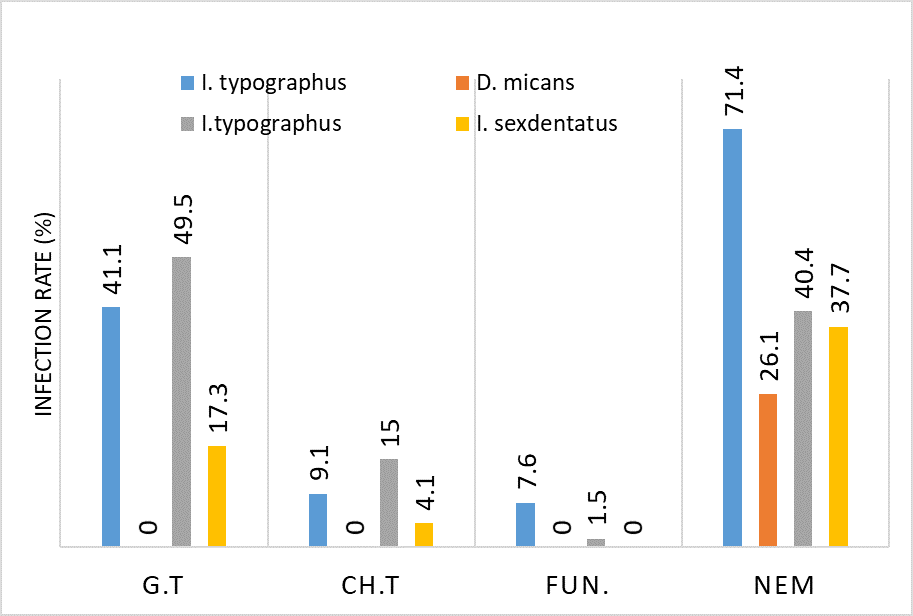
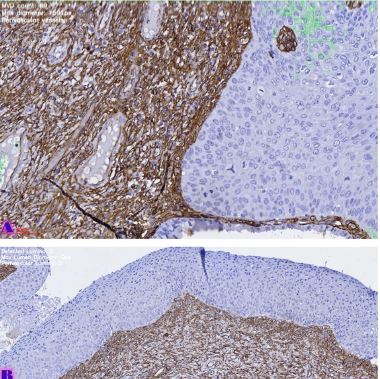
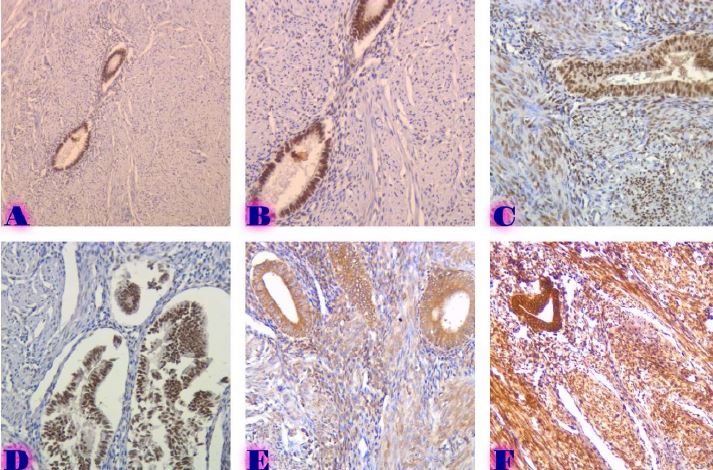
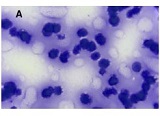
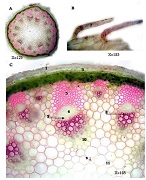
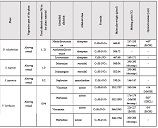
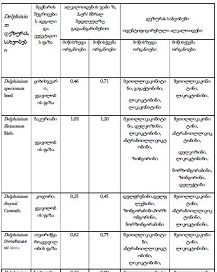
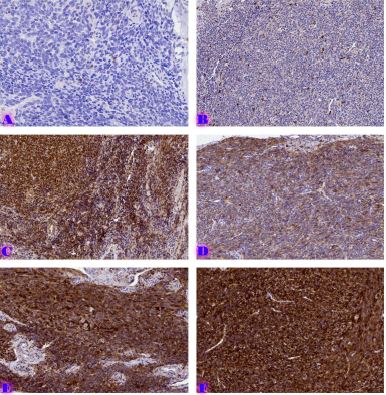
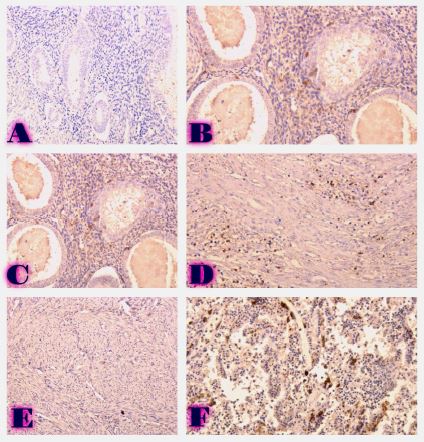
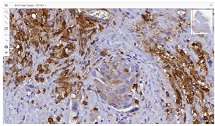
ამ კვლევის მიზანი იყო CD163-დადებითი მაკროფაგების ინფილტრაციის შეფასება საკვერცხის სეროზული სიმსივნეების სპექტრში და მათი სივრცითი განაწილების ანალიზი პერიტონურ იმპლანტებში. რეტროსპექტულად გაანალიზდა სულ 42 შემთხვევა, მათ შორის სეროზული მოსაზღვრე სიმსივნეები, დაბალი ხარისხის სეროზული კარცინომა და მაღალი ხარისხის სეროზული კარცინომა. CD163-ის გამოსავლენი იმუნოჰისტოქიმიური კვლევა ჩატარდა ფორმალინით ფიქსირებულ, პარაფინში ჩაყალიბებულ ქსოვილის ანათლებზე. ციფრული მთლიანი სლაიდის ვიზუალიზაცია (WSI) და რაოდენობრივი ანალიზი გამოყენებული იქნა მაკროფაგების სიმკვრივის (უჯრედები/მმ²) შესაფასებლად წინასწარ განსაზღვრულ კომპარტმენტებში, მათ შორის სტრომულ უბნებში, სიმსივნის ცენტრში, ინვაზიურ ფრონტზე და სიმსივნე-სტრომის ინტერფეისში.
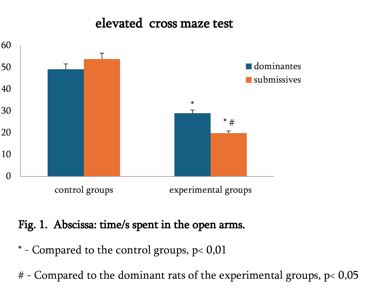
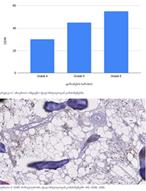
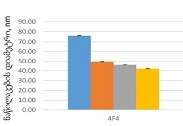
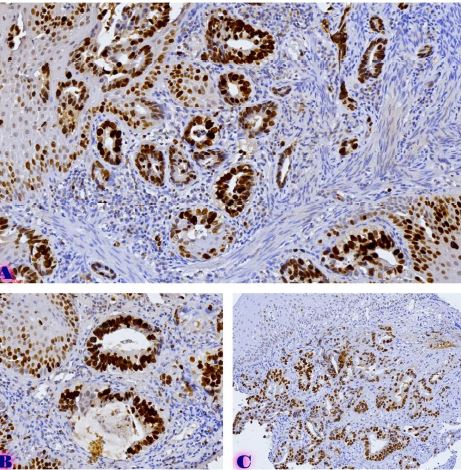
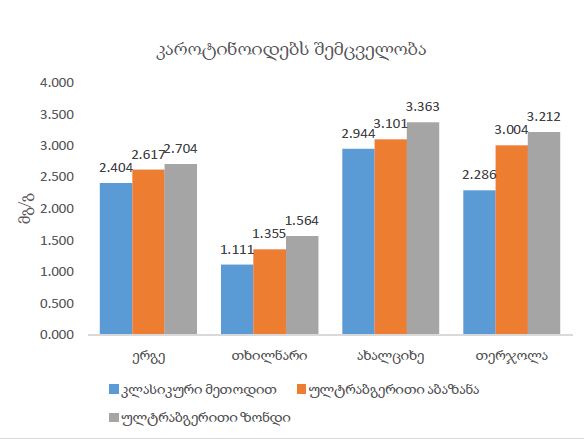
CD163-დადებითი მაკროფაგების სიმკვრივის სტატისტიკურად მნიშვნელოვანი ზრდა დაფიქსირდა მთელ ჰისტოლოგიურ სპექტრში, ყველაზე დაბალი მაჩვენებლებით მოსაზღვრე სიმსივნეებში და ყველაზე მაღალი ხარისხის სეროზულ კარცინომაში. ყველაზე გამოხატული განსხვავებები გამოვლინდა სტრომულ კომპარტმენტში, ინვაზიურ ფრონტზე და სიმსივნე-სტრომის ინტერფეისში (p < 0.001). სივრცულმა ანალიზმა აჩვენა მაკროფაგების უპირატესი დაგროვება პერისიმსივნურ რეგიონებში, რომლებიც დაკავშირებულია ინვაზიასთან, ხოლო სიმსივნის ცენტრის რეგიონებში დაფიქსირდა შედარებით დაბალი სიმკვრივე. გამოვლინდა ძლიერი კორელაცია მაკროფაგების სიმკვრივეებს შორის სტრომულ და ინვაზიურ კომპარტმენტებში, რაც მიუთითებს კოორდინირებულ მიკროგარემოს რემოდელირებაზე.
ეს დასკვნები აჩვენებს CD163-დადებითი მაკროფაგების პროგრესულ მატებას და სივრცით გადანაწილებას საკვერცხის სეროზული სიმსივნეების პერიტონურ იმპლანტანტებში. კვლევის შედეგები ადასტურებს მაკროფაგებით განპირობებული იმუნური მოდულაციისა და სტრომული ურთიერთქმედების როლს სიმსივნის პროგრესირებასა და მეტასტაზურ გავრცელებაში. CD163-დადებითი მაკროფაგების სივრცითი რაოდენობრივი შეფასება შეიძლება ღირებულ ინფორმაციას გვაწვდიდეს სიმსივნის ბიოლოგიის შესახებ და წარმოადგენს პოტენციურ მიდგომას საკვერცხის კიბოს მიკროგარემოზე დაფუძნებული რისკების სტრატიფიკაციისთვის.
Downloads
Devadze R, Gvenetadze A, Burkadze G, Kepuladze S. Distribution of tumor-associated macrophages and M1/M2 polarization in different types and grades of ovarian tumors. Indian Journal of Pathology and Oncology Journal homepage: www.ijpo.co.in Original Research Article [homepage on the Internet] 2022 [cited 2026 Apr 30];9(4):318–321. Available from: https://doi.org/10.18231/j.ijpo.2022.076
Heidarpour M, Hoseini-Beheshti M-S, Id M, Derakhshan ID. Evaluation of the relationship between CD163 positive macrophages and prognostic factors in serous ovarian tumors. Immunopathol Persa [homepage on the Internet] 2020 [cited 2026 Apr 30];6(2):23. Available from: www.immunopathol.comm
Hagemann T, Wilson J, Burke F, et al. Ovarian Cancer Cells Polarize Macrophages Toward A Tumor-Associated Phenotype. The Journal of Immunology 2006;176(8):5023–5032.
Duluc D, Corvaisier M, Blanchard S, et al. Interferon-γ reverses the immunosuppressive and protumoral properties and prevents the generation of human tumor-associated macrophages. Int J Cancer 2009;125(2):367–373.
Alvero AB, Montagna MK, Craveiro V, Liu L, Mor G. Distinct Subpopulations of Epithelial Ovarian Cancer Cells Can Differentially Induce Macrophages and T Regulatory Cells Toward a Pro-Tumor Phenotype. American Journal of Reproductive Immunology 2012;67(3):256–265.
Alvero AB, Chen R, Fu HH, et al. Molecular phenotyping of human ovarian cancer stem cells unravel the mechanisms for repair and chemo-resistance. Cell Cycle 2009;8(1):158–166.
Biswas SK, Gangi L, Paul S, et al. A distinct and unique transcriptional program expressed by tumor-associated macrophages (defective NF-κB and enhanced IRF-3/STAT1 activation). Blood 2006;107(5):2112–2122.
Schutyser E, Struyf S, Proost P, et al. Identification of biologically active chemokine isoforms from ascitic fluid and elevated levels of CCL18/pulmonary and activation-regulated chemokine in ovarian carcinoma. Journal of Biological Chemistry 2002;277(27):24584–24593.
Kryczek I, Zou L, Rodriguez P, et al. B7-H4 expression identifies a novel suppressive macrophage population in human ovarian carcinoma. Journal of Experimental Medicine 2006;203(4):871–881.
No JH, Moon JM, Kim K, Kim YB. Prognostic significance of serum soluble CD163 level in patients with epithelial ovarian cancer. Gynecol Obstet Invest 2013;75(4):263–267.
Chen R, Alvero AB, Silasi DA, Mor G. Inflammation, cancer and chemoresistance: Taking advantage of the toll-like receptor signaling pathway. American Journal of Reproductive Immunology 2007;57(2):93–107.
Kulbe H, Chakravarty P, Leinster DA, et al. A dynamic inflammatory cytokine network in the human ovarian cancer microenvironment. Cancer Res 2012;72(1):66–75.
Reinartz S, Schumann T, Finkernagel F, et al. Mixed-polarization phenotype of ascites-associated macrophages in human ovarian carcinoma: Correlation of CD163 expression, cytokine levels and early relapse. Int J Cancer 2014;134(1):32–42.
Torroella-Kouri M, Silvera R, Rodriguez D, et al. Identification of a subpopulation of macrophages in mammary tumor-bearing mice that are neither M1 nor M2 and are less differentiated. Cancer Res 2009;69(11):4800–4809.
Zhang M, He Y, Sun X, et al. A high M1/M2 ratio of tumor-associated macrophages is associated with extended survival in ovarian cancer patients. J Ovarian Res 2014;7(1).
Robinson-Smith TM, Isaacsohn I, Mercer CA, et al. Macrophages mediate inflammation-enhanced metastasis of ovarian tumors in mice. Cancer Res 2007;67(12):5708–5716.
Neyen C, Plüddemann A, Mukhopadhyay S, et al. Macrophage Scavenger Receptor A Promotes Tumor Progression in Murine Models of Ovarian and Pancreatic Cancer. The Journal of Immunology 2013;190(7):3798–3805.
Tomšová M, Melichar B, Sedláková I, Šteiner I. Prognostic significance of CD3+ tumor-infiltrating lymphocytes in ovarian carcinoma. Gynecol Oncol 2008;108(2):415–420.
Mantovani A, Sozzani S, Locati M, Allavena P, Sica A. Macrophage polarization: Tumor-associated macrophages as a paradigm for polarized M2 mononuclear phagocytes. Trends Immunol 2002;23(11):549–555.
Zhorzholiani P, Bokhua Z, Kepuladze S, Burkadze G. The Role of M1 and M2 Macrophages in the Progression of Endometrial Hyperplasia to Endometrioid Adenocarcinoma. Georgian Scientists [homepage on the Internet] 2025 [cited 2026 Apr 30];7(1):24–37. Available from: https://journals.4science.ge/index.php/GS/article/view/3371
Takaishi K, Komohara Y, Tashiro H, et al. Involvement of M2-polarized macrophages in the ascites from advanced epithelial ovarian carcinoma in tumor progression via Stat3 activation. Cancer Sci 2010;101(10):2128–2136.
Kawamura K, Komohara Y, Takaishi K, Katabuchi H, Takeya M. Detection of M2 macrophages and colony-stimulating factor 1expression in serous and mucinous ovarian epithelial tumors. Pathol Int 2009;59(5):300–305.
საავტორო უფლებები (c) 2026 ქართველი მეცნიერები

ეს ნამუშევარი ლიცენზირებულია Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 საერთაშორისო ლიცენზიით .